
2024年已經結束,如果要從創新藥角度做一份總結,什麽賽道、哪類成分的藥物「最受歡迎」?答案一定是以GLP-1為靶點的各類藥物。
GLP-1原本是作用於2型糖尿病的關鍵靶點,用於治療糖尿病。但在國內社交媒體上,關於司美格魯肽(GLP-1類藥物)的減肥奇效,甚至引發了一股搶藥風潮,甚至有人靠偽裝成糖尿病人,獲取還沒有獲批減肥適應癥的最新藥物。
此外,GLP-1在心血管風險控制方面已經驗證有效,同時在多個其他適應癥領域如腎病、肝病、阿爾茲海默癥、外周動脈疾病等方面也初步獲得驗證。
GLP-1靶點在降糖的套用就像「手榴彈」,但透過減肥的靶點讓它變成了「核彈頭」級別的產品。GLP-1受體激動劑成為了減肥藥物研發領域中最受關註的"靶點",引發了全球新一輪的減肥藥物研發熱潮。
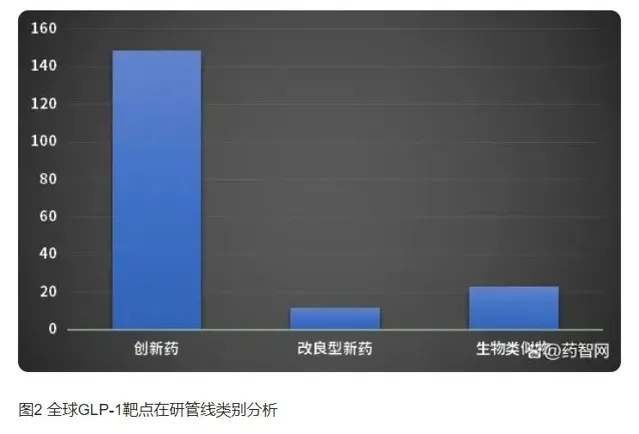
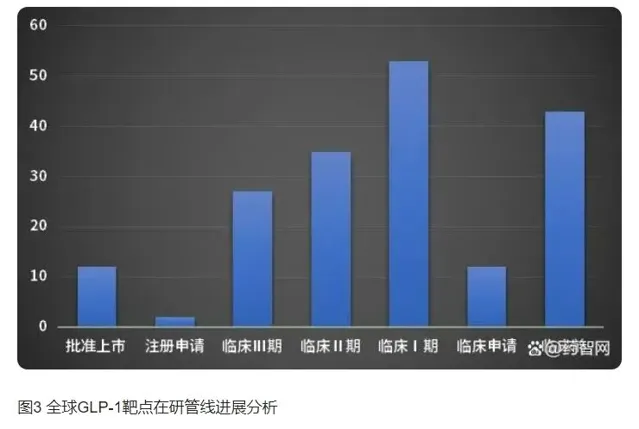
根據天風國際研究報告及藥智數據統計,截至2023年8月,全球GLP-1靶點在研管線有184項,涉及企業133家,涵蓋93個適應癥。共有106個GLP-1類減肥新藥的臨床試驗專案,其中有43個來自中國企業,占比約為40%。市場對GLP-1類減肥藥物的研發也表現出了極高的興趣和熱情。
GLP-1以其在降糖和減重領域明顯的臨床優勢,逐步從抗糖領域轉為減重領域的主流,同時向其它功能輻射!
GLP-1到底是什麽?
為何醫藥業對它趨之若鶩?
GLP-1的發展史
GLP-1(胰高血糖素樣肽-1)的發展史可以追溯到20世紀初。1902年,Starling和Bayliss發現了促胰液素(secretin),這是發現的第一種具有激素功能的物質。1932年,La Barre首次提出「腸促胰素」這一概念,用於描述一種可降低血糖但不會引起胰腺外分泌的腸道上段黏膜萃取物。
到了1960年代,研究者們發現,盡管靜脈註射葡萄糖可達到比口服葡萄糖更高的血糖水平,但口服葡萄糖刺激胰島素分泌反應的效應大於靜脈註射葡萄糖,這種額外效應被稱為「腸促胰素效應」。這一發現為後來的GLP-1的發現和研究奠定了基礎。
1970年代,Brown從小腸黏膜中分離出一種腸促胰素——葡萄糖依賴性促胰島素分泌多肽(GIP)。隨後,在1985年,胰高血糖素樣肽-1(GLP-1)也從腸黏膜中被分離提取出來,成為被證實的第二種也是迄今為止發現的最後一種腸促胰素。
GLP-1的定義與目前已知的功能靶點
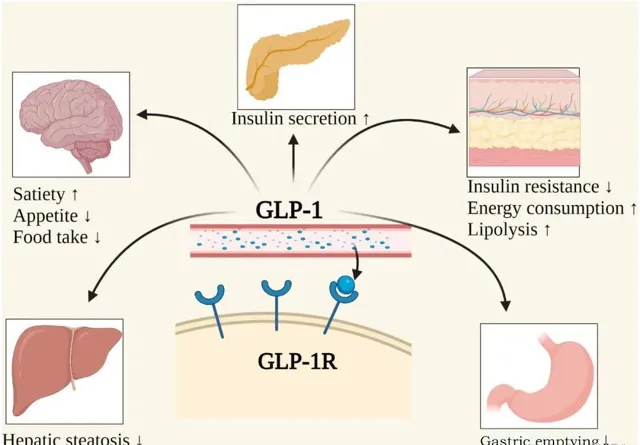
GLP-1(胰高血糖素樣肽-1)是一種腸促胰素,由腸道L細胞分泌,能夠以葡萄糖濃度依賴的方式促進胰島素分泌。在血糖升高時,GLP-1透過與胰島β細胞的GLP-1受體結合,刺激胰島素分泌,降低血糖。同時,GLP-1還可以抑制胰島α細胞分泌胰高血糖素,進一步降低血糖。
同時GLP-1可以促進胰島素分泌,透過啟用神經系統中的GLP-1受體,GLP-1有延緩胃排空和抑制下丘腦攝食中樞的作用,可以增強飽腹感並抑制能量攝入,減少脂肪積累,從而達到減肥的效果。
GLP-1 類藥物在心衰治療方面也具有一定的作用。GLP-1可以透過抑制心臟細胞的雕亡、促進心臟細胞的再生等途徑,保護心臟功能,改善心衰患者的生存質素。
GLP-1類藥物在降血糖的臨床表現
先為達生物公布了Ecnoglutide(XW003)的兩項2期臨床和一項1c期臨床數據。
Ecnoglutide(GLP-1類藥物)治療成年2型糖尿病患者2期研究。受試者接受每周一次皮下註射目標劑量為0.4 mg、0.8 mg、1.2 mg的Ecnoglutide或安慰劑治療,持續20周。在治療20周時,Ecnoglutide組的受試者糖化血紅蛋白(HbA1c)較基線顯著降低1.81% 至2.39%,安慰劑組則降低0.55%(P<0.0001)。治療結束時,81%的Ecnoglutide組受試者實作HbA1c<7%,安慰劑組為19%;33%的Ecnoglutide組受試者體重較基線降低≥5%,安慰劑組為3%。
GLP-1類藥物在減重的臨床表現
在減重方面,50mg 口服司美格魯肽(GLP-1類藥物)治療肥胖或超重的 III 期 OASIS 1 研究在 5 月 22 日宣告成功並釋出數據,6 月發表於 Lancet。
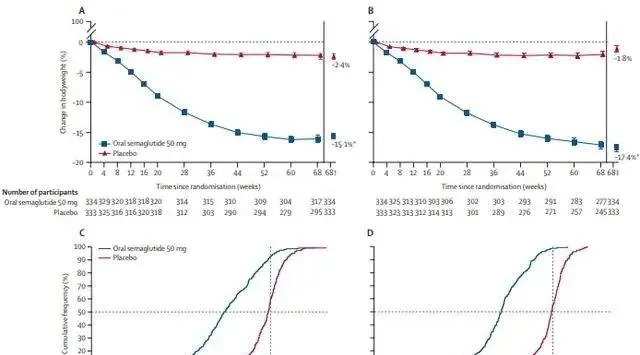
(圖片來源:The Lancet)
結果顯示,口服司美格魯肽在第 68 周時具有統計學意義和更好的體重減輕,達到了其主要終點。平均基線體重為 105.4 公斤,治療組在 68 周實作了 17.4% 的減重效果,而安慰劑組則為 1.8%;此外,89.2% 的口服司美格魯肽組患者在 68 周時體重減輕 ≥ 5%,而安慰劑組僅 24.5%。
補充GLP-1與直接補充胰島素的區別?

在2型糖尿病的治療過程中,經常會發現使用胰島素促泌劑(磺脲類、格列奈類)藥物,以及直接註射胰島素是會導致部份患者變胖。這就與胰島素本身增多會增加脂肪累積風險有關。
但是GLP-1則不一樣, 它是一種人「吃飯後」自然的胃腸激素,所以它不僅對胰島素分泌刺激得更加「自然」,關鍵是,它同時讓你少吃。

同時GLP-1由於模擬人體自然的腸促胰島素激素來調節血糖,其降血糖作用依賴於患者血糖濃度,用藥後不易引起低血糖。
透過調節腸道菌群平衡,
可促進體內GLP-1自然分泌
由於GLP-1是腸道L細胞分泌,所以是可以透過調節腸道菌群平衡,來合理刺激GLP-1分泌,讓身體自然飽足,從而改善、平衡血糖,並且起到一定的抑制肥胖作用。
中創益科聚焦於「糖脂代謝」改善的功能性益生菌菌株,致力於透過益生菌提高內源性代謝力。挖掘能夠刺激內源性GLP-1分泌的益生菌並探究其機制,是中創益科研究的重點,也是中創益科篩選「降糖」菌株的關鍵條件。
具有調節GLP-1分泌能力的益生菌體外篩選
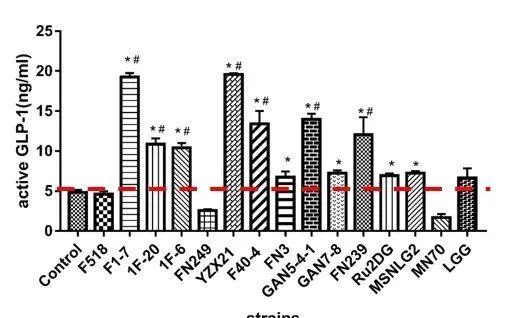
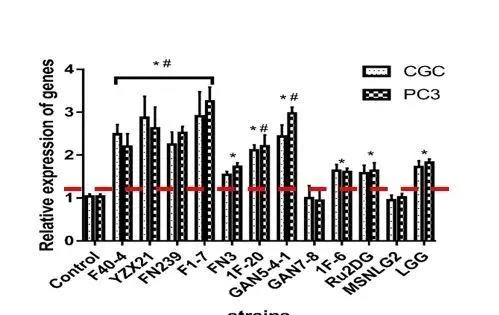
透過構建STC-1細胞,測定益生菌調節GLP-1的能力。觀察到,動物雙歧桿菌F1-7 組的 GLP-1 分泌量最高,為19.66±0.18ng/ml 顯著效果最為突出。植物乳植桿菌YZX21與其相差無幾,緊隨其後。動物雙歧桿菌F1-7對 GCG 和 PC3 基因表現影響顯著,上調倍數均超過 2 倍,顯著高於其他各組,這表明動物雙歧桿菌F1-7和植物乳植桿菌YZX21是我們篩選到2株高表達GLP-1的菌株!
F1-7 及YZX21對2型糖尿病GLP-1分泌及基因表現的影響
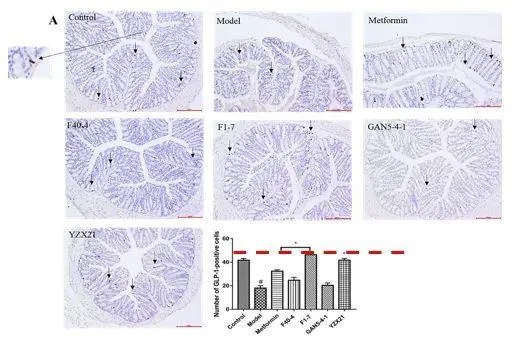
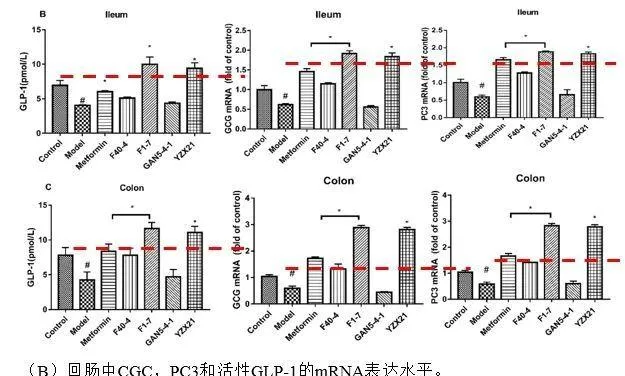
糖尿病小鼠腸道內GLP-1含量減少,F1-7組可增加GCG和PC3基因表現,恢復GLP-1陽性細胞數量,增加結腸中的GLP-1含量,從4.23 pmol/L 增長到 11.65 pmol/L 。YZX21同樣所差無及,說明F1-7及YZX21都能透過調控腸道GLP-1分泌,改善2型糖尿病。
F1-7與YZX21不僅提高內源性GLP-1的基因表現,更可以恢復受損的細胞形態。

糖尿病小鼠胰島細胞體積減少,說明動物雙歧桿菌F1-7與植物乳植桿菌YZX21幹預可恢復細胞形態。

糖尿病小鼠的胰島素訊號減少,胰島血糖素增加。說明動物雙歧桿菌F1-7與植物乳植桿菌YZX21胰島素分泌增加,胰高血糖素分泌降低。
綜上,動物雙歧桿菌F1-7及植物乳植桿菌YZX21與可透過保護胰島細胞,改善胰島素分泌,降低機體胰島素抵抗。
以上實驗數據表明,中創益科動物雙歧桿菌F1-7與植物乳植桿菌YZX21可以增加內源性GLP-1的分泌,並透過GLP-1的功能靶點達到改善2型糖尿病的作用。
總結
1. 以GLP-1為靶點的藥物在降糖與減肥上表現優異,但是它不是躺瘦神器,它僅僅能模擬「吃飽」的狀態,無法改善營養缺失導致的各類病癥。
2.透過調節腸道菌群可以刺激GLP-1分泌,定期的攝入可以緩解2型糖尿病,並減輕肥胖癥狀。
以GLP-1為功能靶點的藥物在持續開發中,讓糖尿病患者與肥胖人群充滿期待與希望。但比起藥物類外源性的GLP-1補充,透過腸道菌群內源性的促進其產生,不失為一個更安全穩妥的辦法。











