基因突變在生物界廣泛存在,除了DNA復制錯誤造成堿基的替換、插入或缺失等自發突變外,一些外界因素如某些化學物質、紫外線、游離輻射等也可能誘導基因突變或損傷。
DNA在復制過程中的錯配事件是不可避免的,前進演化過程賦予DNA聚合酶具有從3'向5'的外切酶活性,可以將DNA復制過程中的錯誤機率控制在10-8的水平上,然而大量研究表明,DNA復制後的錯配機率僅有10-11。[1]
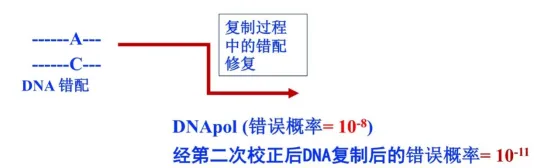
顯然,在DNA復制過程中錯配堿基在逃逸DNA聚合酶的辨識與校正後,還會受到另一機制的檢測,使基因發生突變的可能性降到最低範圍內。
而這將歸功於生物在長期前進演化過程中形成的一套DNA損傷或突變的修復機制。以下將介紹DNA損傷後的幾種典型的修復型別。
【光修復】
科學家在原核生物、植物、動物細胞中都發現了光修復現象。
紫外線照射可造成細胞內DNA單鏈上形成嘧啶二聚體(以胸腺嘧啶二聚體最常見),破壞了DNA雙鏈間的堿基配對,造成DNA不能成為復制或轉錄的樣版。
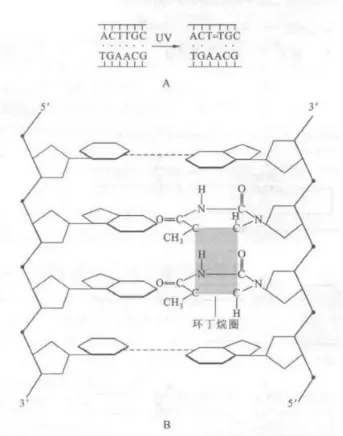
這時光復合酶結合到DNA的損傷部位二聚體處,在可見光(最有效波長為400nm)的作用下,光復合酶被啟用,切斷二聚體之間的兩個C-C鍵,酶解離的同時使嘧啶二聚體變成兩個單體,最終使DNA又恢復正常的結構和功能[2]。
【切除修復】
切除修復也可以消除由紫外線、游離輻射、化學誘變劑等引起的DNA損傷。
它是指在幾種酶的協同作用下,先在DNA損傷的一端切開磷酸二酯鍵,然後切除一段寡核苷酸,留下的缺口由DNA聚合酶I根據堿基配對的原則來填補,最後再由連線酶將缺口補齊。
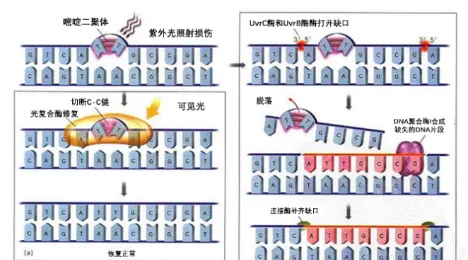
可見,以上兩種修復方式都能 使DNA分子恢復正常。
【重組修復】
重組修復在大腸桿菌中首次發現,可用「拆東墻、補西墻」形象地比喻這種修復機制。
當紫外線照射造成大腸桿菌細胞內DNA單鏈上形成T二聚體,以T二聚體為樣版 復制的子代DNA分子上會留下空缺部位。
隨後,在RecA酶的作用下,將另一DNA分子樣版鏈的對應區域透過交換置換到空缺處,再以正常單鏈DNA為樣版,重新合成DNA以填補置換後形成的新空缺。
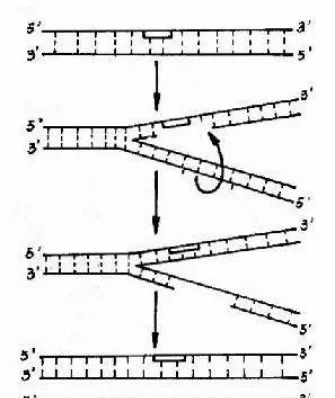
可見,這種依靠鏈的置換方式來進行修復,它不可能對空缺部位進行準確的片段轉移,因此這種修復系統僅是以「保證填補DNA空缺、避免個體死亡」為目的的修復機制。
【SOS(搶救)修復】
SOS修復是DNA受到嚴重損傷,細胞處於危急狀態時所誘導的一種消耗大量能量的修復機制,在λ噬菌體中首次發現。λ噬菌體中的SOS修復系統主要由RecA(輔蛋白酶)和LexA(基因的阻遏物)進行調控。
正常情況下, LexA 基因的編碼產物是一種具有較廣泛生理效應的阻遏蛋白,它不僅對自身基因的表達具有負調控效應,而且對 RecA 基因以及能誘發突變的 UmuC 相關基因也具有負調控的抑制效應。
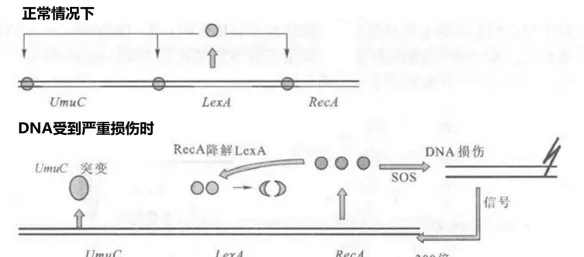
當DNA分子受到嚴重損傷時,斷裂遊離的單鏈DNA片段作為一種重要的訊號分子,使RecA蛋白啟用出能降解LexA阻遏蛋白的蛋白酶活性,消除其負調控活性,而且能誘導 RecA 基因以高於正常條件下300倍以上的效率進行轉錄,進而使重組修復機制啟動,催化空缺部位DNA的合成[1]。
這時的DNA的損傷只能得到「傾向差錯」的修復,也就是說,這時補上去的核苷酸幾乎都是隨機的, 修復結果只能維持基因組的完整性,提高細胞的生成率,但留下較多錯誤,使細胞有較高的突變率。
【總結】
綜上所述,細胞的修復系統是DNA分子的一種安全保障體系,這種修復有 準確的,避免錯誤的修復 ,也有以 保證個體存活,順利透過DNA復制的「傾向差錯」 的修復,對於生物個體的生存繁衍,前進演化具有重要意義。
參考文獻
[1]鄭用璉主編;羅傑,胡南副主編.基礎分子生物學 第3版[M].北京:高等教育出版社.2018.
[2]李菡,吳慶余編.基礎生命科學[M].北京:高等教育出版社.2006.











