肝癌是全球第六大最常見的癌癥,每年大約有90.5萬例新發病例,其中85%~90%為肝細胞癌。尤其以中國肝癌發病率高,據統計,中國原發性肝癌的發病和死亡例數占比分別占全球的54.6%和53.9%,毫不誇張地說, 中國基本上以全球20%的人口認領了超過50%的肝癌患者。
不僅肝癌具有高死亡率,而且早期肝癌極難發現。 9成以上一經發現就已是晚期,此時已失去了手術治療的機會,致使5年生存率僅為12%,中晚期肝癌患者的5年生存率更是低至3%。
中晚期肝癌患者一般已經不具有手術移植的價值,而細胞免疫治療方式能夠幫助患者提升機體免疫力,同時對於腫瘤細胞存在極強的殺傷力,對於惡性腫瘤屬於一種新的治療方式。
近年來,免疫療法作為手術、放療和化療之後的「第四種療法」,可謂是風頭正盛!尤其是細胞免疫療法在肝癌方面的臨床研究一直都從未停歇,有望打破中國肝癌患者多年來的「枷鎖」!
作為一種 「活的」藥物 ,嵌合抗原受體T細胞(CAR-T 細胞)療法與傳統藥物有著很大的區別。 它是一種治療腫瘤的新型精準靶向療法。透過基因工程技術將T細胞啟用,並裝上定位導航裝置CAR(腫瘤嵌合抗原受體),將T細胞這個普通「戰士」改造成「超級戰士」,即CAR-T細胞,專門辨識體內腫瘤細胞,並高效殺滅腫瘤細胞,從而達到治療惡性腫瘤的目的。 與傳統的化療和造血幹細胞移植相比,它對腫瘤細胞的殺傷更為精準,在提高療效的同時大幅減輕了毒副作用。
CAR-T療法首次套用於血液系統惡性腫瘤,取得了令人鼓舞的結果,同時,其在實體腫瘤治療的套用中也展現出積極的效果,顯示出 CAR-T細胞治療巨大的潛力和發展前景。隨著基礎研究的深入、治療理念的更新,已有研究將CAR-T細胞治療套用於原發性肝癌。
今天無癌家園小編就列舉些目前國內外已經發表的關於CAR-T療法治療肝癌的臨床研究,以供各位癌友們參考。
晚期肝癌患者無癌超3年!國研靶向GPC3的CAR-T療法突飛猛進
2022年8月18日,科濟藥業宣布,【Frontiers in Immunology】雜誌上發表了關於其自主研發的靶向GPC3的CAR-T細胞候選產品CT011治療晚期肝細胞癌的長期生存案例報告。

該研究團隊是最早報道了GPC3是CAR-T治療的理想靶點,且率先開展CAR-T治療肝細胞癌的臨床試驗。此項研究報道了 1名晚期肝細胞癌患者在接受GPC3 CAR-T細胞與索拉非尼聯合治療後獲得了完全緩解(CR)和長期生存。
這是一名患有B型肝炎病毒(HBV)相關肝細胞癌的60歲男性,於2018年5月接受手術,2018年8月術後發生肝癌復發並出現肺轉移,隨後又進行了經動脈化療栓塞治療(TACE)處理肝部病竈和介入消融處理肺部轉移。不幸的是,在2018年11月6日出現疾病進展,有幸符合臨床試驗入組條件。在入組後,該名患者接受單采制備GPC3 CAR-T細胞。在單采後7天,患者開始服用索拉非尼,400mg/次,2次/d。患者接受了4個周期的GPC3 CAR-T細胞(CT011)治療,每個周期分為兩次輸註。在接受CT011治療的每個周期之前,進行清淋化療預處理。共輸註4×109 個GPC3 CAR-T細胞。
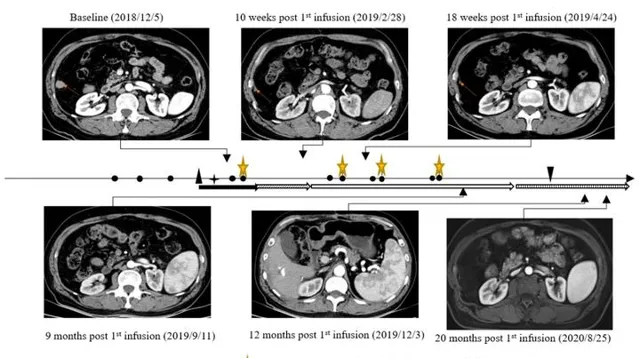
(影像顯示大面積凝固斑塊壞死、外周纖維化、慢性炎性細胞浸潤、無明顯腫瘤殘留,表明抗腫瘤治療後有反應)
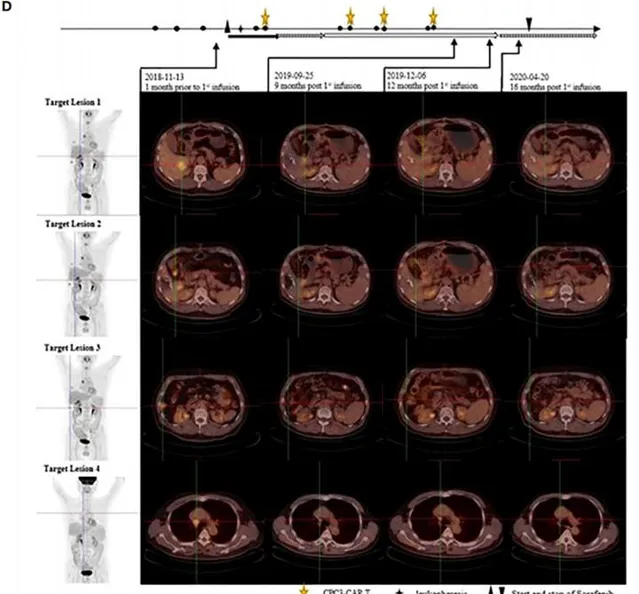
(患者在基線時接受PET-CT檢查,首次輸註後6、9、12、16個月。1號、2號和3號靶病變在第12個月消失,而4號靶病變病變不活躍,在抗腫瘤治療後被認為是非特異性攝取)
CT011聯合索拉非尼治療耐受性良好。 患者從第3個月開始達到部份緩解(PR), 並 在第一個 CT011 輸註周期後的第12個月達到完全緩解 。 腫瘤超過36個月沒有進展,在第一次輸註後保持完全緩解狀態超過24個月。
據悉,這是CAR-T細胞與酪胺酸激酶抑制劑聯合治療後報告的第一個完全緩解病例。臨床結果表明, GPC3 CAR-T細胞與索拉非尼的聯合治療,可能成為治療GPC3表達陽性的晚期肝細胞癌患者的一種有前景的療法。
好訊息是,這種新型的CAR-T療法在國內已正式開始招募患者了,主要評估CAR-GPC3 T細胞療法在≥18 歲復發或難治性晚期肝細胞癌患者中的安全性及療效。
想要參加的患者可送出病理報告、治療經歷、出院小結等資料至無癌家園醫學部初步評估病情。
【入組標準(部份)】
1.年齡18~75歲;
2.至少有一個可評估的病竈;
3.組織病理學或細胞學診斷為晚期肝細胞癌 (HCC) 的患者;先前標準全身治療後的進展或不耐受;免疫組化(IHC)檢測GPC3陽性
疾病控制率達78%,國產CAR-T療法在肝癌領域大展拳腳
2021年6月4日,一年一度的美國ASCO(美國臨床腫瘤學會)年會上中國醫學研究者們首次公布了 靶向GPC3的CAR-T藥物(Ori-CAR-001) 治療 復發/難治性肝細胞癌 的最新臨床研究數據。該研究的初步數據顯示, Ori-CAR-001在GPC3陽性復發/難治性患者中表現出良好安全性和有效性。
截至2021年3月10日,共納入11名接受細胞輸註的復發受試者。 所有受試者均患有晚期肝細胞癌,並且經過化療、TACE(肝動脈化療栓塞術)和靶向治療均無效。 按照巴塞隆納分期標準,除了1例為 B期(中期)外,其余10例受試者均為 C期(晚期)。所有受試者均有多處轉移病竈,其中 6 例(54%)有肺部等遠處轉移。2例受試者提前退組無法評估。剩余的9例可評估受試者中, 4例達到部份緩解 (PR),3例達到疾病穩定 (SD),2例出現疾病進展 (PD),客觀緩解率為44%,疾病控制率達到78%。
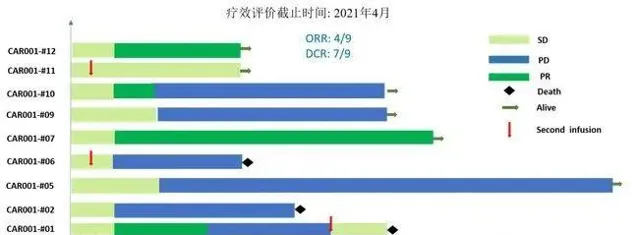
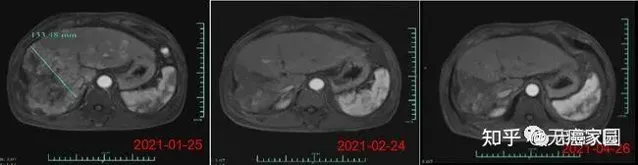
在數據截止時,受試者007的部份緩解時間6個月, 其腫瘤體積在細胞治療輸註後1個月減少了80%以上。 (截至2021年6月,該受試者已超過8個月的疾病控制,隨訪仍在進行中)。受試者012是1例彌漫型、巨塊型晚期肝癌患者,曾接受過12次以上的TACE治療、放療及靶向治療,不幸的是均無效,隨後參與本研究。
在輸註CAR-T細胞後的第28天, 受試者MRI結果顯示最大腫瘤直徑從最初的133公釐減少至9公釐,縮小超過93%。 目前, 該受試者正在接受CAR-T細胞輸註後第3個月的評估,MRI掃描顯示此腫瘤幾乎消失。 此外,甲胎蛋白(AFP,原發性肝癌的特定腫瘤標誌物)水平從基線值 >80,000/ng/ml 下降到第1個月的1148.9ng/ml,並在第3個月下降到746.7ng/ml輸註(正常範圍<40ng/ml),證明Ori-CAR-001在晚期肝癌患者中具有顯著的初步療效。
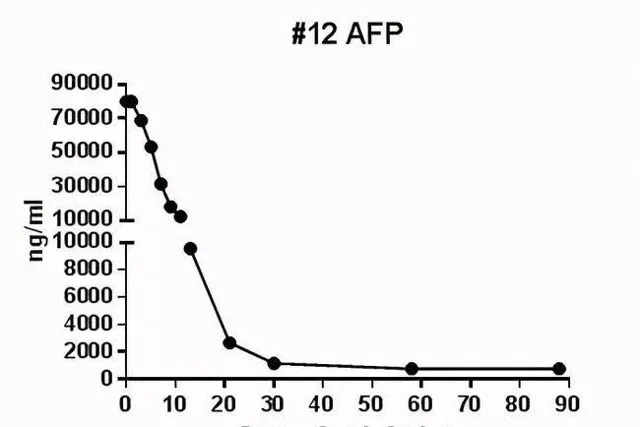
在已回輸的11例患者中,Ori-CAR-001顯示出了良好的安全性和耐受性。9例患者觀察到了細胞因子釋放症候群(CRS),其中7例發生1-2級CRS,2例經靜脈回輸出現4級CRS,給予類固醇激素和托珠單抗治療後恢復正常。沒有觀察到神經毒性。
改造特殊CAR-T技術,讓晚期肝癌、胰臟癌病竈通通消失!
針對CAR-T細胞進入腫瘤組織困難、CAR-T細胞進入腫瘤組織後容易被其他免疫抑制性的分子或細胞所阻擋無法發揮作用等問題,中國的醫學研究者想到的辦法是讓CAR-T細胞同分時泌細胞因子和趨化因子。這些因子好比給CAR-T細胞配置了一個內建的能量馬達,能夠增強CAR-T細胞進入腫瘤內部的能力。
2021年7月29日,國際知名雜誌【Journal of Hematology & Oncology】刊登了中國醫學研究者們的一項成功改造CAR-T技術的臨床研究,研究中提及的CAR-T產品選擇的靶點是 glypican-3(GPC3)和mesothelin(MSLN) ,為了使CAR-T細胞具有更強的進入腫瘤內部的能力,研究人員特地加裝了白介素7(IL-7)和趨化因子CCL19。
此次研究納入的是6例具有 GPC3或MSLN表達的晚期肝細胞癌(HCC)、胰臟癌(PC)和卵巢癌(OC)患者 。治療結果格外令人驚艷!
其中1例晚期肝癌患者接受了瘤內註射CAR-T治療,治療後肝臟病竈代謝基本消失。
更絕的是1例晚期胰臟癌患者,接受的是靜脈回輸的CAR-T治療,治療後全身的病竈,基本都實作了代謝活性完全消失。
典型病例01
具有GPC3表達的晚期肝細胞癌患者
受試者GD-G/M-001是一例具有GPC3表達的晚期肝細胞癌患者,在研究中選擇3個轉移性病變進行電腦斷層掃描(CT)引導的CAR-T細胞的瘤內註射。
CAR-T細胞 註射60天後 ,雖然2個肺部結節的尺寸沒有顯著的改變,但在 第10天時肝臟腫瘤病變(1.2×1.3cm)顯著收縮 , 註射GPC3-7×19 CAR-T細胞第32天後則完全消失。
患者沒有任何毒性作用,並且根據 CT 上的標準實體瘤反應評估標準 (RECIST) 1.1 版進行了分期評估,顯示部份緩解 (PR)。
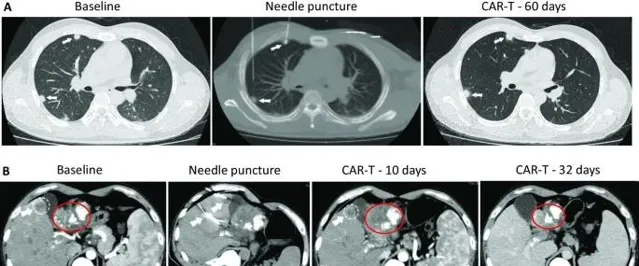
02 具有MSLN表達的晚期胰臟癌患者
受試者GD-G/M-005 是一例具有 MSLN 表達的晚期胰臟癌患者。該受試者進展為局部淋巴結轉移(24×33 mm)(圖c)。抗 MSLN-7 × 19 CAR-T 細胞首先透過肝動脈輸註,當晚伴有高燒,沒有細胞因子釋放症候群 (CRS) 或神經毒性。隨後,他每1~2個月接受一次抗 MSLN-7×19 CAR-T 細胞的靜脈輸註。
直到增至CAR-T細胞輸註的5倍,CT分期顯示 他在治療240天後達到完全緩解, 測定的淋巴結為8.3×9.6mm, 並未見其他腫大的淋巴結 (圖C), 患者此時病竈完全消失,保持正常狀態。
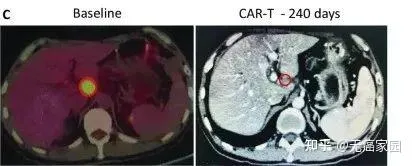
中國研發全球第一個靶向GPC3的CAR-T療法,初戰告捷
在2020年5月5日的國際權威期刊【Clinical Cancer Research(臨床腫瘤研究)】上,刊登了上海研究人員完成的世界第一個針對GPC3靶點治療晚期肝癌的探索性CAR-T臨床試驗。

在兩項前瞻性I期研究中,患有晚期GPC3 + HCC的成年患者(Child-Pugh A)在環磷醯胺和氟達拉濱誘導的淋巴清除後接受了自體CAR-GPC3 T細胞療法。主要目的是評估治療的安全性。
截止到2019年7月24日,共有13例患者接受了中位值為19.9×108的CAR-GPC3 T細胞。所有患者均為GPC3陽性,均接受過手術治療、局部治療或全身性的系統治療,都攜帶B型肝炎病毒(HBV)。
其中有2例患者獲得部份緩解(PR),所有患者6個月、1年和3年的生存率分別為50.3%、42.0%和10.5%,中位生存時間(OS)為278天(39.7周)。
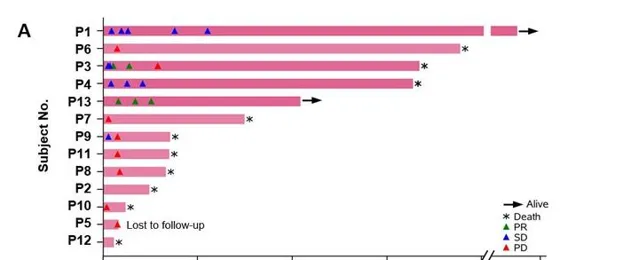
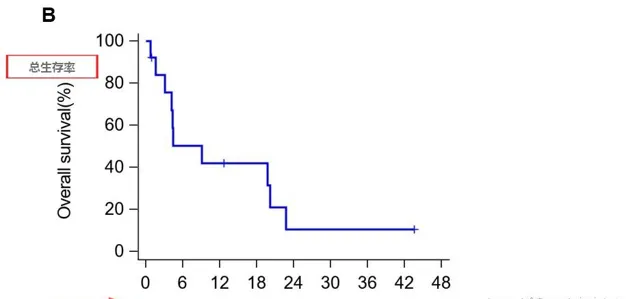
典型病例
這兩例患者生存時間分別是20.5個月(圖P13)和44.2個月(圖P3) ,其中 一例疾病穩定的患者至今生存期將近4年 ,他在入選時已有下腔靜脈癌栓、右心房癌栓以及淋巴結轉移,治療後AFP(甲胎蛋白)長期維持正常水平且長期生存。
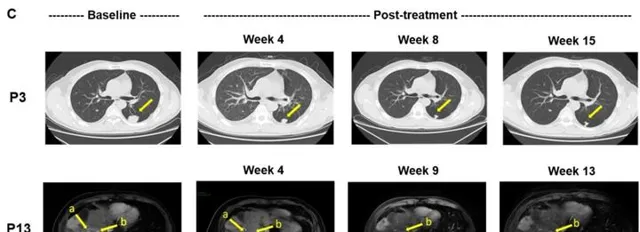
安全性
在安全性方面,主要是細胞因子釋放症候群(CRS),其中8名患者出現了可逆可控的1/2級CRS,1名患者經歷了5級CRS。
臨床過程中,沒有出現3/4級的神經毒性事件。
研究證明了CAR-GPC3 T細胞療法的初步安全性與療效性,值得後續深入研究。
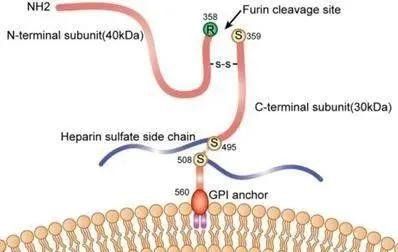
GPC3到底是什麽靶點?具有何意義?
磷脂酰肌醇蛋白聚糖3(glypican 3,GPC3)在調控細胞生長和分化方面起重要作用,與肝癌的發生、發展密切相關。GPC3在肝細胞癌、卵巢透明細胞癌、卵黃囊癌等生殖系統腫瘤中表達, 其在肝細胞癌中的表達率達74.8%,而在正常肝組織內幾乎無表達,稱為肝癌CAR-T治療新的理想靶點。
GPC3因其腫瘤特異性,被認為是極有前景的腫瘤免疫治療靶標。這表明在肝細胞癌中GPC3的表達越高,預後越差。
除了肝癌患者外,目前無癌家園還急招B細胞淋巴瘤、T細胞淋巴瘤、T細胞白血病(T-ALL)、急性白血病、非霍奇金淋巴瘤、胃癌、前列腺癌、甲狀腺癌、間皮瘤等癌種的患者!
任重道遠,CAR-T療法將為更多實體瘤患者帶來新的希望!
截至目前,國內開展的CAR-T臨床試驗數量已經超過500項,居世界第一,這也是中國首次在一個新藥研發領域走到國際前列。其中,傳奇生物的西達基奧侖賽、斯丹賽生物的GCC19CART、科濟藥業的Claudin18.2 CAR-T都達到全球領先水平。此外,還有多公司在布局新一代CAR-T以及異體CAR-T技術,初步數據優異,有望獲得全球市場。
2021年中國迎來了細胞免疫治療的元年,作為先鋒的CAR-T療法,是未來發展方向之一。CAR-T療法主要在於改造T細胞來使其辨識腫瘤細胞的特殊靶點,理論上,可以有無數種針對不同靶點的CAR-T療法,這意味著蘊含著無限可能。
希望不久的將來,能夠在國內外醫學科研工作者的努力下,降低細胞療法毒副作用,降低價格,突破實體瘤的瓶頸,讓越來越多的晚期癌癥患者獲益!
本文為無癌家園原創










