撰文 | 姬智
在精神病學發展的行程中,有一些發現至關重要,甚至從根本上改變了這個學科的面貌。比如佛洛伊德的精神分析學說;Ugo Cerletti發明的電抽搐治療(Electroconvulsive therapy,簡稱「ECT」);John Cade發掘了鋰鹽作為精神科藥物的套用價值等等。而在這些改變遊戲規則的發現中,大名鼎鼎的「百憂解」(Prozac)無疑牢牢占據了一席之地。
百憂解,主要成分為氟西汀 (Fluoxetine),是第一個成功上市的選擇性5-羥色胺 (5-HT)再吸收抑制劑 (SSRI,Selective Serotonin Reuptake Inhibitors) 類抗抑郁藥,其藥物形態為鹽酸氟西汀 (Fluoxetine hydrochloride) 。
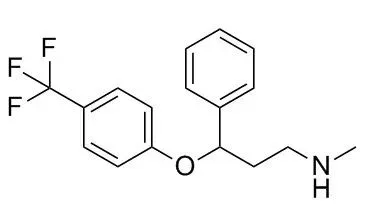
圖1. 鹽酸氟西汀化學結構
氟西汀由禮來(Eli Lilly)公司於1972年發現,1987年被美國FDA批準用於治療抑郁癥,給當時被抑郁癥困擾的患者們帶來了希望。也是從氟西汀開始,陸陸續續有SSRI類抗抑郁藥上市,它們開辟了抑郁癥藥物治療的新篇章,成為最廣泛使用的抗抑郁類處方藥。三十年悄然流逝,越來越多的基於新機制新靶點的抗抑郁藥物登上市場舞台,但氟西汀在臨床中依然十分常用,它是世界衛生組織所列出的基本藥物之一,也是基本衛生系統必不可少的重要藥品 [1] 。
抗結核藥物的「副作用」
抗抑郁藥物的研究起源最早要追溯到20世紀50年代先驅Nathan S. Kline的工作。Kline是紐約羅克蘭縣羅克蘭醫院的研究主任(Rockland Hospital in Rockland County,New York),當時結核病肆虐,臨床醫生們在使用抗結核藥物治療病人的過程中,意外發現了此類藥物對病人有一種神奇的心理影響——它可以使病人表現出「不同尋常」的快樂。報道引起了Kline的註意,他開始進行自己的抑郁癥藥物研究,並與精神分析家Mortimer Ostow在1957年的美國精神病學協會年會上聯合發表了這方面的報告 [2] ,獲得了當時學術界的認可。大家開始相信,藥物治療也能為抑郁癥患者帶來希望。自此,一種新的藥物類別——抗抑郁藥——誕生了。
早期的抗抑郁藥物多為三環類抗抑郁藥 (Tricyclic antidepressants,TCAs)。這類藥物最早正是由抗結核藥物改造而來,其核心結構為一個七元雜環,兩邊各連線一個苯環。它可以抑制突觸前膜對去甲基腎上腺素(NA)和五羥色胺(5-HT) 的再攝取,增加二者在突觸間隙中的濃度,以延長它們作用於相應受體的時間,從而發揮抗抑郁作用。
三環類的代表藥物有丙咪嗪、阿米替林、氯丙咪嗪、多塞平、地昔帕明、去甲替林、普羅替林等(圖2)。其中阿米替林對伴失眠的抑郁患者療效較好;丙咪嗪對內源性抑郁癥、更年期抑郁癥患者更為理想,對精神病的抑郁癥狀效果較差;而氯丙咪嗪是治療強迫癥的首選藥物,同時也是美國 FDA 批準的治療強迫癥的藥物之一;多塞平則對各類焦慮抑郁狀態效果較好 [3] 。
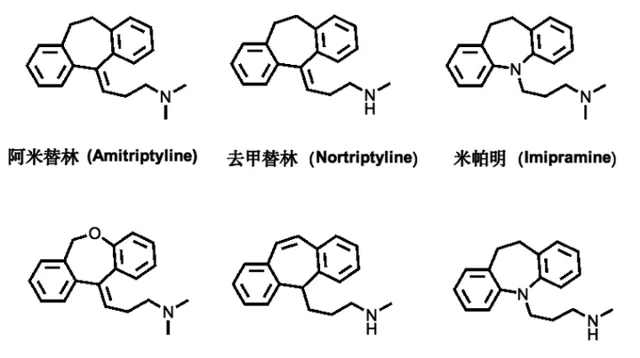
圖2. 常見的三環類抗抑郁藥 (Tricyclic antidepressants,TCAs)
三環類藥物雖然被證實具有抗抑郁的效果,但也具有較為明顯的毒副作用。例如,治療安全窗小,有嚴重的心臟毒性,有抗膽堿作用(表現為口幹、便秘、視物模糊、嗜睡、體重增加等),會引起體位性低血壓等。因此,科學家們一直致力於研發毒副作用更小、療效更好的藥物。
生理學發展指明新方向
藥物的發展離不開生理學研究的推動 。早期分析抑郁癥病人的屍檢樣本時,科學家們就已經發現,在自殺死亡的抑郁癥病人後腦中,5-羥色胺(5-HT)和其代謝物 5-羥基-吲哚乙酸(5-HIAA)的水平要比突發性死亡或心肌梗死病人低得多 [4, 5] ,這是否意味著人體內5-HT水平可能與抑郁癥有關?
1969年,一本名為【神經組織的結構和功能】 ( The Structure and Function of Nervous Tissue, Volume III: Biochemistry and Disease )的書出版,書中詳細介紹了當時中樞神經生理學的「最新」知識 [6] ,詳細闡述了5-HT在人體內的合成、儲存、釋放、分解和再攝取的過程,這些過程符合5-HT作為神經傳導物質的標準。同時,藥理學也有證據證明,與NA相似,5-HT與抑郁癥的病理密切相關。受此啟發,科學家們轉而開始尋找毒性較小的單胺傳導物質再攝取抑制劑,期望透過特定地抑制5-HT的再攝取來改善抑郁癥狀。
現在我們知道,5-羥色胺(5-HT)也稱作血清素(Serotonin),是一種單胺類神經傳導物質。同屬於這個家族的還有多巴胺(Dopamine, 簡稱「DA」)、去甲基腎上腺素(Norepinephrine,簡稱「NE」或「NA」) 等等,這些神經傳導物質都能在神經元中合成,並能介導神經訊號傳遞,因此也與人類的情緒調節有關。
隨著生物學科的發展,現代設計新藥往往基於已經確定的作用靶標,借助於強大的電腦輔助功能,來設計合成有作用的先導化合物。而回到1960年代,在當時生理學水平有限的情況下,科學家們能從抑郁癥病人屍檢樣本分析中,敏銳地觀察到5-HT水平與抑郁癥的關聯,並開創性地提出「選擇性再攝取抑制劑」的概念,在當時確實是了不起的成就。
何為再攝取抑制劑?5-HT在突觸前神經元細胞中合成,釋放進入突觸間隙,與突觸後神經元上的受體家族結合,進而介導神經訊號傳遞。在此過程中,突觸前神經元上的再攝取泵會將一部份遊離的5-HT再次攝取,導致5-HT濃度降低。
SSRIs正是透過抑制再攝取泵來發揮作用,它使得突觸間隙的5-HT濃度升高。相似的作用原理,三環類抗抑郁藥可以同時抑制突觸前膜對NA和5-HT的再攝取,不具有選擇性;而氟西汀則只選擇性抑制5-HT的再吸收,並不影響多巴胺與去甲基腎上腺素的生理作用,這也是它的優勢之一。
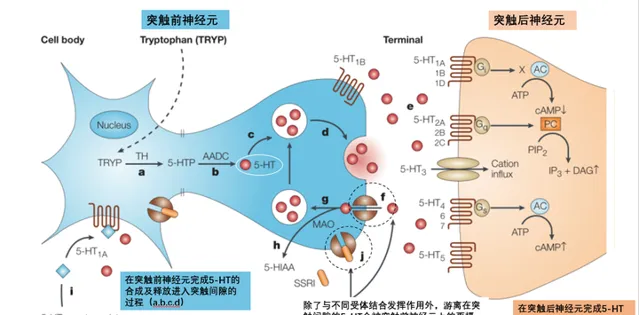
圖3. 5-HT及SSRIs的作用機制【7】
不如人意的結構改造
1970年,禮來的藥物化學家Bryan Molloy和藥理學家Robert Rathburn開始合作,目的是開發一種新型抗抑郁藥物,既能夠保留三環類抗抑郁藥物(TCAs)的治療活性,又能夠克服TCAs的心臟毒性和抗膽堿能作用。基於早期TCAs研究的基礎,他們采取了藥物誘導的小鼠體溫降低模型對藥物進行篩選,發現苯海拉明 (Diphenhydramine) 和其它一些抗組織胺類藥物也達到了和TCAs相同的效果。瑞典郭德堡大學(University of Goteborg)的Arvid Carlsson和同事們則觀察到,苯海拉明除了拮抗組織胺受體外,還能抑制單胺攝取,後者意味著它在治療抑郁癥方面可能會有效果 [8] 。
基於上述發現, Molloy對苯海拉明進行結構改造及最佳化,合成了許多類似物。在第一輪改造時,他們保持了含有N-甲基乙基胺的側鏈不變,將苯海拉明的N,N-二甲基-2-(二苯基甲氧基)-乙胺結構演變為苯氧基苯胺母核,設計合成了一系列3-苯氧苯丙胺基化合物,並在Rathbun實驗室對這批新合成的分子進行藥理測試,發現化合物LY94939 (又稱Nisoxetine,漢譯「尼索西汀」) 具有與TCAs類抗抑郁藥物相同活性。而之後的體外靶點活性測試表明,尼索西汀與地昔帕明一樣,對去甲基腎上腺素有再攝取抑制作用,而對5-羥色胺(5-HT)和多巴胺 (DA)的再攝取抑制作用則微弱很多 [9, 10] 。因此,科學家們繼續探索,試圖找到可以針對5-HT進行抑制的藥物分子。
然而,這樣的探索並不被看好,甚至受到了多方阻撓。例如,一位中樞神經系統研究方面的學術專家,在每季度存取禮來公司時,都勸他們打消追求單胺攝取選擇性抑制劑的念頭,因為當時其他科學家的觀點是,增強5-HT的再攝取不僅無法治療抑郁癥,反而可能會導致抑郁。但研究團隊沒有放棄,幸虧有禮來CNS(Central Nervous System)研究委員會顧問Slater的支持,這個計畫總算沒有中斷。
氟西汀:纖毫之差
我們必須知道的一個事實是,藥物化學是一門非常精妙的學科,即使只有細微的結構差別,兩個分子的藥效也會有很大區別 。在這個計畫中,結構的細微變化也會改變分子對不同神經傳導物質的選擇。
1971年,另一位推動氟西汀誕生的重要人物——David T. Wong——加入了研究團隊。Wong出生於中國香港,是當時著名的生物化學家,過去的科研經歷讓他十分熟悉5-HT對情緒調節的作用。在他的鼓勵下,研究小組又設計合成了第二批50多個化合物,並將這兩批化合物再次進行篩選,以尋找可能選擇性抑制5-HT再攝取的分子。研究小組對這兩批化合物重新進行了體外5-HT、NA、DA再攝取抑制活性測試,發現化合物LY82816(氟西汀的草酸鹽形態)對5-HT再攝取表現出了非常好的選擇性 [11] 。
其實,氟西汀與同一系列的化合物結構差別非常小。下圖(圖4)是這類化合物的構效關系總結,我們可以看出,3-苯氧苯丙胺基化合物中2個苯環均無取代時,其對5-HT和NA的再攝取抑制活性 (Ki) 分別為102nM和200nM。而在苯氧基對位引入三氟甲基 (即氟西汀)後,對5-HT再攝取抑制活性提高了6倍 (Ki=17nM) 。不僅如此,正如上文所提到的, 氟西汀還具有較強的靶點選擇性,這意味著,氟西汀在抑制5-HT再攝取的同時,不會幹擾其他神經傳導物質的正常功能。
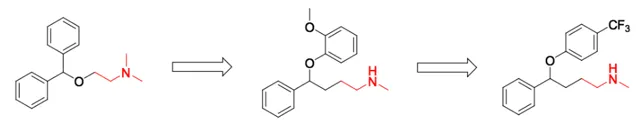

圖4. 改造過程中系列化合物的構效關系
重建動物模型
誰知,與尼索西汀不同,氟西汀在藥物誘導的小鼠體溫降低模型中竟然沒有顯示出活性!原來,這一時期普遍采用的抗抑郁癥研究的動物模型是建立在早期三環類抗抑郁藥的基礎上的,因而特別適用於抑制去甲基腎上腺素(NA)再攝取類藥物,但對氟西汀卻無法顯示出顯著的體內活性。當務之急,研究者需要建立5-HT在體內的再攝取抑制模型。
經過不斷摸索,Wong等科學家們建立了三種新的模型來評估氟西汀的抗抑郁活性。這三種動物模型分別是,小鼠強迫遊泳實驗 (Forced swim test);習得性無助模型 (learning helpless) 和嗅球切除模型 (Olfactory bulbectomy)。在這三種模型中,氟西汀都表現出了良好的效果,最終使大家認可了氟西汀。在此之後,這三種模型得到了廣泛使用。
臨床一波三折
最終,1976年,在動物體內的安全性實驗全部完成之後,禮來公司向FDA送出了臨床研究申請,首次對人服用氟西汀進行臨床實驗研究。一期臨床進展非常順利,氟西汀表現出良好的臨床安全性,很快就準備好進入第二階段:尋找治療抑郁癥患者的有效性指標。
在當時,禮來公司還有其他更靠前的候選藥物需要考察,加之缺乏精神病學方面經驗豐富的臨床研究人員,氟西汀的臨床二期試驗一度陷入僵局。在資源有限的情況下,二期臨床一開始只能以一個相對小的規模進行。然而,不幸的事再次發生了:在這一批小規模人群中,氟西汀被發現無效!
這給整個計畫組帶來了極大的打擊。好在,研究小組經過分析之後,認為試驗失敗可能要歸咎於誌願患者的型別——因為這批患者在先前的治療中對其他抗抑郁療法也沒有反應。大家振作精神,繼續推進,在另一群抑郁癥患者中重新開始試驗,終於取得了良好的結果。
1981年,氟西汀的臨床III期試驗開始,於1983年順利完成。結果顯示,氟西汀對抑郁癥療效顯著,且副作用輕。這些試驗的臨床結果組譯在100多卷2英寸的活頁夾中,送出給美國FDA,用於申請上市。從第一次人體給藥,到完成所有的試驗,送出材料,一共花費了七年多的時間 [12] 。
但是,對氟西汀和研究團隊的考驗還沒有結束。
遭遇藥物搶發
幾乎同一時間,1982 年,阿斯利康制藥公司(Astra Pharmaceuticals)在歐洲率先推出了治療抑郁癥的藥物齊美利定 (Zimelidine)。無獨有偶,齊美利定也是一種選擇性 5-HT 再攝取抑制劑 (SSRI) [13] 。禮來公司失去了第一個向市場推出SSRI的機會。
然而,齊美利定上市後不久,就曝出會引發一些罕見的副作用,尤其是引發類流感症候群。為了避免更大的損失,阿斯利康立即終止了有關 SSRI 的所有研究。這無疑送給了禮來一線生機。
1983年 10月,禮來公司研發團隊代表與 FDA 咨詢委員會會面,期望他們能綜合評價氟西汀的臨床研究結果及獲批上市的可能性。兩年後,也就是1985年10月,FDA咨詢委員召開會議,討論氟西汀的上市申請。雖然有人質疑氟西汀可能產生類似於齊美利定引發的流感樣反應,但咨詢委員會成員認為,兩者結構有明顯區別,這種特殊的副作用可能是齊美利定特有的,並一致建議批準使用氟西汀治療抑郁癥。
在研究團隊焦急的等待中,1987年 12月29日,FDA 終於批準鹽酸氟西汀上市。1988年1月,禮來公司以商品名「Prozac (百憂解)」 成功推出 5-HT 再攝取抑制劑氟西汀,用於治療抑郁癥(圖4)。研究團隊多年來承受的壓力與質疑,終於在此刻被歡樂代替。
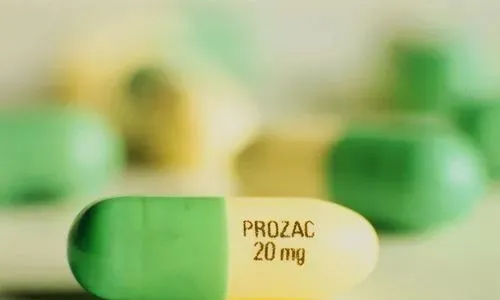
圖5. 禮來公司成功推出 5-HT再攝取抑制劑氟西汀,商品名取為Prozac(百憂解)丨圖片來源:https:// images.app.goo.gl/8Lmz3 p4kAts7iYr9
氟西汀療效確切,副反應輕,上市之後廣受歡迎,銷售額連年增長,1988年全球銷售額突破1億美元,1992年突破10億美元大關,成為第一個年銷售額突破10億美元大關的中樞神經系統藥物。1999年銷售額更是達到26.13億美元,為全球第6暢銷藥品。【財富】雜誌( Fortune magazine ) 將氟西汀列為「世紀藥品」之一,2001年專利到期後,專利藥市場銷售額下降明顯,但氟西汀的總處方量未受影響 [14] 。
氟西汀的一戰成名給各大制藥公司指引了新的方向,一大批公司加入5-HT再攝取抑制劑開發的行列,資金註入和研究人員的努力使得短短幾年之內就有帕羅西汀、舍曲林、文拉法辛、西酞普蘭等一系列SSRIs類抗抑郁藥進入市場。給抑郁癥患者帶來了新的希望。
唯有信念
回到開頭,為什麽說百憂解的問世是改變精神病學發展行程的事件之一?除了它良好的抗抑郁效果外,更重要的是,百憂解在一定程度上重塑了公眾對精神障礙的認識,重新定義了臨床抑郁癥的概念,將精神病學的方向從心理治療扭轉為生物學治療。
由於百憂解非常安全,並且與其他藥物之間交互作用的風險極小,所以之前不願開具三環類藥物處方的醫生開始為癥狀較輕的患者使用藥物治療,這在一定程度上解除了當時抑郁癥的汙名化,令更多人敢於吐露自己的病情。因此,百憂解毫無爭議地成為精神病學史上的標誌性藥物,其地位是不可撼動的。
氟西汀的成功問世也給科研人員們留下了寶貴的經驗。研究者在16年的時間裏歷經各種考驗,每一步都極為艱辛。他們的成功經驗為後來的新藥研發提供了非常好的借鑒意義:最初,沒有建立合適的評價模型,導致氟西汀動物體內測試(人體外測試)無效;接著,公司優先發展其他藥物,導致氟西汀臨床研究暫停;同時,病人選擇有誤,導致臨床研究失敗;最後,同類藥物副作用又導致公司決定暫停研發。如果不是研究人員堅韌的毅力和不懈追求真理的精神,氟西汀的研究可能早已夭折。而這種精神,在世人多急功近利的今天顯得尤為可貴。

圖6. 氟西汀研發過程中兩位重要的科學家Bryan B. Molloy 與David T. Wong丨圖片來源:左https://www. invent.org/inductees/br yan-b-molloy ;右:http:// blogs.oregonstate.edu/ )
科學的發展是一個不斷積累的過程。神經科學的先驅們提供了生理學基礎、開創性的設計思路,研究團隊又透過深入的思考和不懈的努力來驗證思路,遭受懷疑、嘲笑也不放棄,才最終取得了突破性的成果。就像David T. Wong在三十年以後回顧氟西汀的研發之路時說的那樣:
It is essential that ideas are steadfastly championed by passionate believers to achieve the final goal.參考資料
[1] https:// apps.who.int/iris/bitst ream/handle/10665/93142/EML_18_eng.pdf;jsessionid=9633BBC4D3838AC972A59899C442C306?sequence=1
[2] Loomer, H. P., Saunders, J. C., & Kline, N. S. (1957). A clinical and pharmacodynamic evaluation of iproniazid as a psychic energizer. Psychiatric Research Reports, 8, 129–141.
[3] Feighner J. P. (1999). Mechanism of action of antidepressant medications. The Journal of clinical psychiatry, 60 Suppl 4, 4–13.
[4] Shaw, D. M., Camps, F. E., & Eccleston, E. G. (1967). 5-Hydroxytryptamine in the hind-brain of depressive suicides. The British journal of psychiatry : the journal of mental science, 113(505), 1407–1411.
[5] Bourne HR, Bunney WE Jr, Colburn RW, et al. Noradrenaline, 5-hydroxytryptamine, and 5-hydroxyindoleacetic acid in hindbrains of suicidal patients. Lancet. 1968;2(7572):805-808.
[6] Bailey OT. The Structure and Function of Nervous Tissue, vol 3, Biochemistry and Disease. JAMA. 1970;212(9):1528–1529. doi:10.1001/jama.1970.03170220082030
[7] Wong DT, Perry KW, Bymaster FP. Case history: the discovery of fluoxetine hydrochloride (Prozac). Nat Rev Drug Discov. 2005;4(9):764-774. doi:10.1038/nrd1821
[8] Molloy, B. B., Wong, D. T . & Fuller, R. W. The discovery of fluoxetine. Pharmaceutical News 1, 6–10 (1994).
[9] Wong, D. T., Horng, J. S., & Bymaster, F. P. (1975). dl-N-methyl-3-(o-methoxyphenoxy)-3-phenylpropylamine hydrochloride, Lilly 94939, a potent inhibitor for uptake of norepinephrine into rat brain synaptosomes and heart. Life sciences, 17(5), 755–760. https:// doi.org/10.1016/0024-32 05(75) 90531-7
[10] Wong DT, Bymaster FP. Effect of nisoxetine on uptake of catecholamines in synaptosomes isolated from discrete regions of rat brain. Biochem Pharmacol. 1976;25(17):1979-1983. doi:10.1016/0006-2952(76)90053-8
[11] Wong DT, Bymaster FP, Horng JS, Molloy BB. A new selective inhibitor for uptake of serotonin into synaptosomes of rat brain: 3-(p-trifluoromethylphenoxy). N-methyl-3-phenylpropylamine. J Pharmacol Exp Ther 1975;193(3):804-11
[12] Wong DT, Bymaster FP, Reid LR, Threlkeld PG. Fluoxetine and two other serotonin uptake inhibitors without affinity for neuronal receptors. Biochem Pharmacol. 1983;32(7):1287-1293. doi:10.1016/0006-2952(83)90284-8
[13] Bengtsson BO, Wiholm BE, Myrhed M, Wålinder J. Adverse experiences during treatment with zimeldine on special licence in Sweden. Int Clin Psychopharmacol. 1994;9(1):55-61. doi:10.1097/00004850-199400910-00009
[14] https://www. psychologytoday.com/us/ blog/freud-fluoxetine/202003/the-story-prozac-landmark-drug-in-psychiatry









