嘗試過減肥的人都知道,減重本身已經很艱難,而維持減重後的體重更是難上加難。
很多人在減肥後不久就會遇到體重反彈的問題,這不僅僅是行為和飲食習慣難以持久改變所致,很多時候,身體本身的機制也在起作用。
最近,【自然】雜誌發表了一篇來自蘇黎世聯邦理工學院科研團隊的研究論文,揭示了肥胖對身體的深遠影響。研究團隊分析了成功減重者的脂肪組織,發現曾經的肥胖狀態導致的細胞轉錄變化在減重兩年後依然存在。

研究人員在小鼠實驗中也發現了類似現象:「胖過」的脂肪細胞更傾向於吸收更多的糖和脂肪,一旦再次接觸到高脂食物,小鼠的體重會更快地恢復到之前的水平。
這項研究使用了來自MTSS、LTSS和NEFA三項減肥手術相關的臨床研究中的脂肪組織樣本,包括手術前(T0)和手術後兩年(T1)的皮下脂肪(scAT)和網膜脂肪(omAT)。所有參與者的BMI至少降低了25%,健康體重者的數據作為對照組。
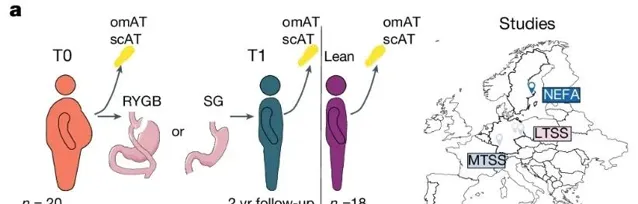
透過單細胞核RNA測序(snRNA-seq)分析發現,網膜脂肪(omAT)樣本中存在18個細胞簇,盡管細胞組成在T0和T1之間沒有顯著差異,但許多在T0時的差異表達基因(DEG)在T1時仍然失調。皮下脂肪(scAT)中也觀察到了類似的結果,表明肥胖引起的脂肪組織細胞轉錄變化在減重後仍未恢復。
進一步的研究發現,肥胖期間的轉錄失調在脂肪細胞、脂肪細胞祖細胞(APC)和內皮細胞中最為明顯。功能上,與脂肪細胞代謝和功能相關的通路下調,而與纖維化和細胞雕亡相關的通路上調。
為了驗證這一發現,研究者在小鼠中進行了實驗。首先,小鼠被餵食高脂飲食(HFD)一段時間以使其變胖,然後改為低脂飲食,讓它們在4-8周內減重至正常體重。結果顯示,大多數肥胖導致的代謝指標在減重後恢復到正常水平,但附睪脂肪(epiAT)中的細胞變化卻不容樂觀。
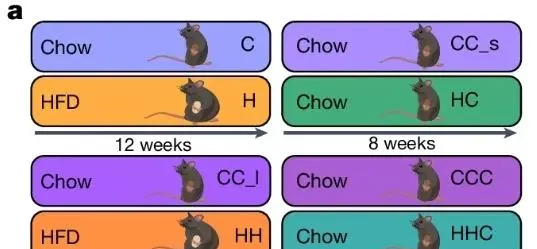
肥胖時,小鼠epiAT中的巨噬細胞數量顯著增加,減重後也沒有減少,尤其是脂質相關巨噬細胞(LAM)和非血管周圍巨噬細胞的數量增加,導致巨噬細胞群結構發生變化。與人類組織的測序結果一致,小鼠epiAT中肥胖導致的DEG在減重後仍然存在,包括溶酶體活性、細胞雕亡和其他炎癥途徑相關基因的上調,以及脂肪代謝相關基因的下調。
有趣的是,研究者發現,餵食HFD時間更長的小鼠在減重後,沒有任何DEG恢復正常表達,情況比餵食HFD時間較短的小鼠更嚴重。這表明,長時間的肥胖或較短的減重時間會強化「胖記憶」。
研究者進一步分析了「胖記憶」的成因,發現主要是表觀遺傳機制在起作用。減重後,57-62%的下調DEG和68-75%的上調DEG都可以用表觀遺傳解釋。

「胖記憶」會導致什麽樣的後果呢?研究者發現,胖過的小鼠的附睪脂肪(epiAT)對葡萄糖和棕櫚酸酯的攝取顯著增加。再次餵食高脂飲食時,這些小鼠的體重恢復速度比從未胖過的小鼠更快。
目前,研究者還不能確定這種肥胖記憶能夠持續多久,或許有一個時間視窗,或許會一直持續。無論如何,這一發現為我們理解肥胖和體重管理提供了新的視角,也為未來的治療策略提供了新的思路。











