表皮生长因子受体(EGFR)作为非小细胞肺癌(NSCLC)中最早发现的驱动基因,可谓真正改变了非小细胞肺癌的治疗格局。表皮生长因子受体-酪氨酸激酶抑制剂(EGFR-TKI)以其高精度和高特异性,实现了「疗效好」和「副反应小」的双赢。
目前,已有三代EGFR-TKI用于临床,包括第一代的吉非替尼、厄洛替尼等,第二代的阿法替尼、达可替尼,第三代的奥希替尼等。
但几乎所有的靶向药物,都面临着巨大的挑战:耐药。即便是「神药」奥希替尼,也难以避免。科学家们不断探索研究耐药机制,希望能够改变靶向药物耐药的局面。
终于,在机制探索过程中,他们发现代谢重编程是正常细胞发生恶性转化的重要特点,可能是靶向药耐药的一大机制。近期,科学家们发现了一个新的逆转EGFR-TKI耐药的靶点——醛糖还原酶(AKR1B1)。癌度和大家一起分享这一最新研究成果。
醛糖还原酶:多代EGFR-TKI耐药的潜在靶点
醛糖还原酶是做什么的呢?当血糖正常时,这种酶不会被激活。然而,在高血糖的环境下,醛糖还原酶就会被激活,将葡萄糖转化为山梨醇,而山梨醇不易透过细胞膜,会在细胞内蓄积,使细胞膜的通透性发生改变,导致细胞代谢与功能的损害。因此,糖尿病病人常常需要使用醛糖还原酶抑制剂来降低这种酶的活性。
醛糖还原酶和EGFR-TKI耐药有什么关系呢?首先,科学家发现醛糖还原酶表达与非小细胞肺癌耐药相关(图1A)。进一步探索发现,无论是厄洛替尼耐药(ER),吉非替尼耐药(GR)还是奥希替尼耐药(OR)的细胞,醛糖还原酶的表达量均明显升高;而且OR细胞醛糖还原酶表达相对更高(图1B)。这些初步结果提示,醛糖还原酶 是多代EGFR-TKI耐药的潜在靶点 。
 图1.AKR1B1与EGFR-TKI耐药相关
图1.AKR1B1与EGFR-TKI耐药相关
醛糖还原酶为什么与多代EGFR-TKI耐药有关呢?随后,科学家进行了深层机制的探索。 EGFR-TKI耐药细胞存在一个奇怪的现象,那就是「谷胱甘肽从头合成」这一细胞代谢明显旺盛了起来 (图2)。

图2.谷胱甘肽从头合成影响EGFR-TKI耐药
敏锐的科学家自然想到,这一代谢是否能和醛糖还原酶这个优选靶点联系起来呢?于是,他们采用一些技术干扰了EGFR-TKI耐药细胞中醛糖还原酶的表达,观察谷胱甘肽合成的量是否变化。结果发现, 醛糖还原酶表达的抑制,会明显减少谷胱甘肽合成 (图3)。进一步研究,科学家发现,醛糖还原酶高表达,通过活化细胞增殖相关的STAT3通路,来促进谷胱甘肽从头合成过程,最终诱导了EGFR-TKI耐药。
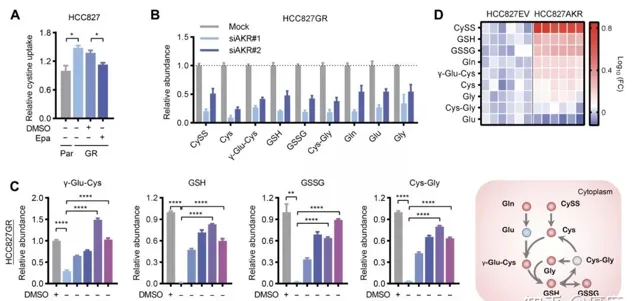 图3.耐药细胞中AKR1B1表达控制谷胱甘肽从头合成过程
图3.耐药细胞中AKR1B1表达控制谷胱甘肽从头合成过程
降糖药依帕司他抑制醛糖还原酶表达,逆转EGFR-TKI耐药
机制清楚了,是否能通过抑制醛糖还原酶来逆转EGFR-TKI耐药,延长EGFR-TKI作用时间呢?这才是我们最为关心的问题。他们想到了依帕司他,这是一种常用的降糖药,同时也是醛糖还原酶的抑制剂。也就是说, 常用降糖药依帕司他能抑制醛糖还原酶表达。如果能证实依帕司他能逆转EGFR-TKI耐药,临床就有可及的廉价药了! 在早期现象观察中,科学家在EGFR-TKI耐药细胞中加入了依帕司他,结果令人惊喜—肿瘤细胞的生长增殖活性被有效抑制了(图4)。
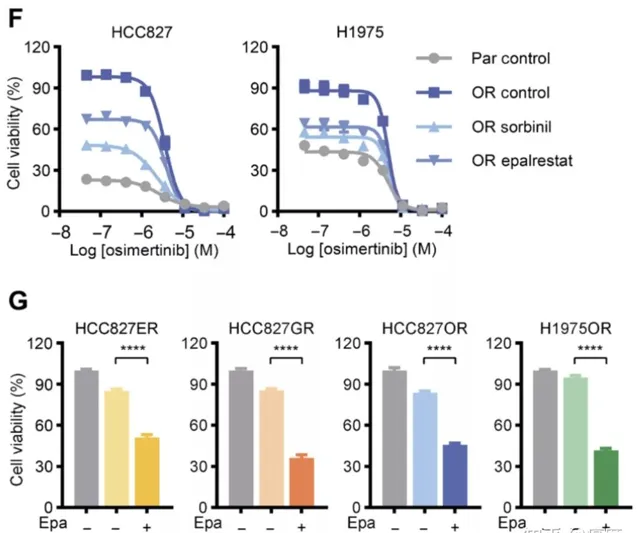 图4.依帕司他有效抑制EGFR-TKI耐药肿瘤细胞的活性
图4.依帕司他有效抑制EGFR-TKI耐药肿瘤细胞的活性
克服重重研究困难后,科学家开始了体内实验研究,这是比单纯细胞层面的结果更为可靠的实验。他们将耐药细胞接种到小鼠体内,观察醛糖还原酶抑制剂依帕司他,以及依帕司他联合奥希替尼,对肿瘤生长的抑制效果。
结果显示, 无论是肿瘤细胞来源的小鼠模型,还是人肿瘤来源的小鼠模型(PDX),依帕司他均能有效延长奥希替尼的治疗效果和有效时间(图5A~E)。将依帕司他与奥希替尼联合应用时,肿瘤体积缩小非常明显,几乎所有肿瘤的治疗疗效都能达到部分缓解(PR),这其中80%病灶几乎消失,达到了完全缓解(CR) (图5F)。免疫组化染色进一步显示,醛糖还原酶导致EGFR-TKI耐药过程中的关键分子,STAT3和SLC7A11得到了有效的抑制(图5G),这从机制层面证实了醛糖还原酶抑制对EGFR-TKI耐药的逆转。
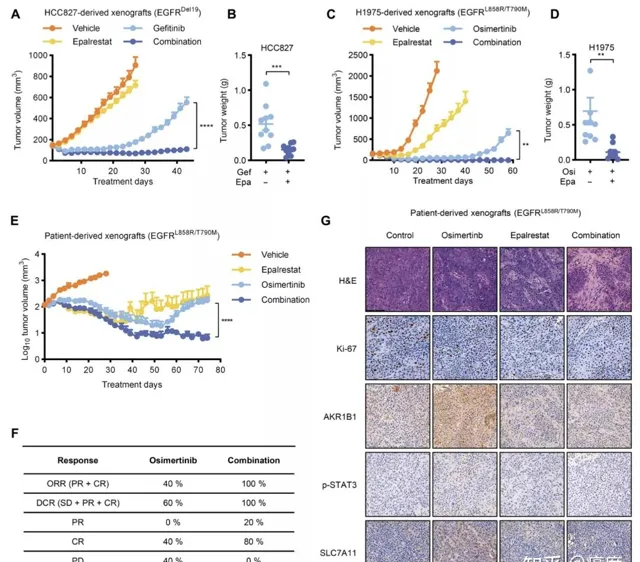 图5.体内实验验证依帕司他通过抑制AKR1B1活性达到逆转EGFR-TKI耐药效果
图5.体内实验验证依帕司他通过抑制AKR1B1活性达到逆转EGFR-TKI耐药效果
小结与启示
一种常用的降糖药依帕司他,能有效逆转EGFR-TKI的获得性耐药发生,这就是这项研究的临床潜在意义。通过检测醛糖还原酶表达情况,对醛糖还原酶高表达的EGFR突变患者加用这一常见的降糖治疗药物,或许能很好地提高EGFR-TKI的抗肿瘤作用,并延长EGFR-TKI的起效持续时间。当然,这还是一项初期的基础研究,依帕司他的临床效果如何,如何设定醛糖还原酶高表达临界值以筛选最佳获益人群等等问题,我们还要期待后续的临床试验。
这项研究从代谢角度,解释了EGFR-TKI获得性耐药的机制和应对策略,丰富了肿瘤靶向治疗耐药机制研究的内涵。相信快速的研究进展,将逐步从多个方面、多个角度阐述靶向治疗的耐药机制,为临床肿瘤患者的个体化治疗提供更加精准的蓝图。











